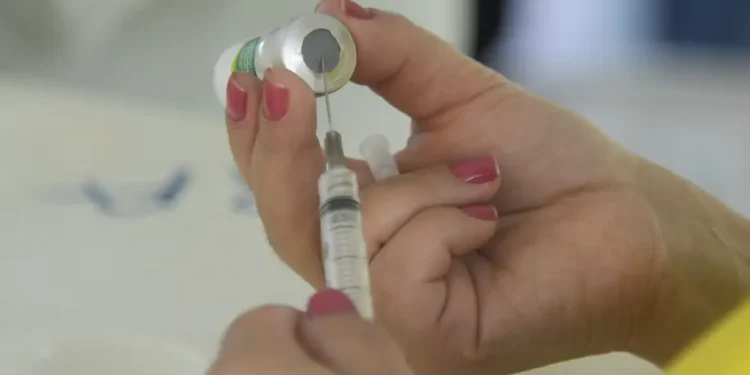
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta segunda-feira (14) a vacina contra chikungunya. O imunizante poderá ser aplicado em pessoas a partir de 18 anos de idade. O pedido foi encaminhado pelo Instituto Butantan, órgão ligado à Secretaria de Estado da Saúde de São Paulo, em parceria com a Valneva, empresa farmacêutica franco-austríaca.
Esta é a primeira vacina autorizada contra a doença, que pode causar dor crônica nas articulações e afetou 620 mil pessoas no mundo só em 2024. Os países com mais casos da doença são Brasil, Paraguai, Argentina e Bolívia.
O imunizante contra a chikungunya já recebeu aprovação nos Estados Unidos e na União Europeia. A vacina foi avaliada nos Estados Unidos em 4 mil voluntários de 18 a 65 anos, tendo apresentado um bom perfil de segurança e alta imunogenicidade.
De acordo com resultados do estudo-clínico publicado na revista científica The Lancet, 98,9% dos participantes do ensaio clínico produziram anticorpos neutralizantes, com níveis que se mantiveram robustos por ao menos seis meses.
De acordo com o Instituto Butantan, o parecer favorável da Anvisa representa um importante passo na aprovação da versão do instituto do imunizante, que já está em análise pela agência reguladora. As duas vacinas têm praticamente a mesma composição e a versão do Instituto Butantan será adequada à possível incorporação no enfrentamento da doença em nível de saúde pública.
No estudo clínico de fase 3 feito com adolescentes brasileiros, publicado na The Lancet Infectious Diseases em setembro de 2024, após uma dose da vacina, foi observada presença de anticorpos neutralizantes em 100% dos voluntários com infecção prévia e em 98,8% daqueles sem contato anterior com o vírus.
A proteção foi mantida em 99,1% dos jovens após seis meses. A maioria dos eventos adversos registrados após a vacinação foi leve ou moderada, sendo os mais relatados dor de cabeça, dor no corpo, fadiga e febre.
Mas para que o produto chegue, de fato na população, alguns passos regulatórios ainda devem ser cumpridos. Instituto Butantan está trabalhando em uma versão com parte do processo realizado no Brasil. As modificações usam componentes nacionais e será melhor adequado à incorporação pelo SUS, pendente análise pela CONITEC, Programa Nacional de Imunizações e demais autoridades de saúde.





